2. 扬州大学附属苏北人民医院急诊科, 扬州 225001
哒螨灵(pyridaben)作为新型杀虫剂,是一种线粒体电子传递抑制剂,中毒后可导致多器官功能损害,尚无特效解毒剂,病死率较高。目前有关哒螨灵中毒致中毒性脑病的临床报道较为少见。本例患者口服哒螨灵中毒后以持续的意识障碍为主要症状,影像学检查符合中毒性脑病表现。现将该患者中毒急性期及出院后随访资料进行总结,旨在为该类中毒性脑病的临床诊疗与预后提供参考。
1 病例资料患者男,67岁,既往有糖尿病史,2023-07-05口服农药哒螨灵约50 mL,具体浓度不详。服药10 h后出现行走不稳,被家属送至当地医院行清水洗胃10 000 mL,随后出现意识不清、血压下降,诊断为急性哒螨灵中毒并紧急转至我院。入急诊查体:血压65/40 mmHg(1 mmHg=0.133 kPa),深昏迷,格拉斯哥昏迷指数(GCS)3分(E1V1M1), 双侧瞳孔等大等圆,直径3 mm,对光反射迟钝,颈软,双侧鼻唇沟对称。双肺呼吸音粗,未闻及啰音。心律齐,心率103次/min。生理反射存在,病理反射未引出。完善实验室检查,动脉血气分析:pH 6.973,氧分压112.4 mmHg,二氧化碳分压22.6 mmHg,乳酸15.5 mmol/L;血常规:白细胞计数25.81×109/L, 中性粒细胞百分比80.9 %;生化指标:丙氨酸氨基转移酶62.0 U/L,门冬氨酸氨基转移酶129.0 U/L,肌酐151.30 umol/L;心肌损伤标记物:肌钙蛋白I 1.24 ng/mL,肌酸激酶同工酶16.03ng/mL,肌红蛋白 > 600.0 ng/mL。血液药物浓度检测(采用液相-质谱联1用仪):哒螨灵浓度为120 ng/mL。入院后立即行气管插管接呼吸机辅助呼吸、多巴胺泵入升压[8 ug/(kg·min)]。入院当日胸部CT:两肺少许炎症、渗出,右侧胸腔少量积液。头颅CT:双侧脑室旁见对称性月晕状稍低密度影,颅内多发缺血灶,见图 1A。
|
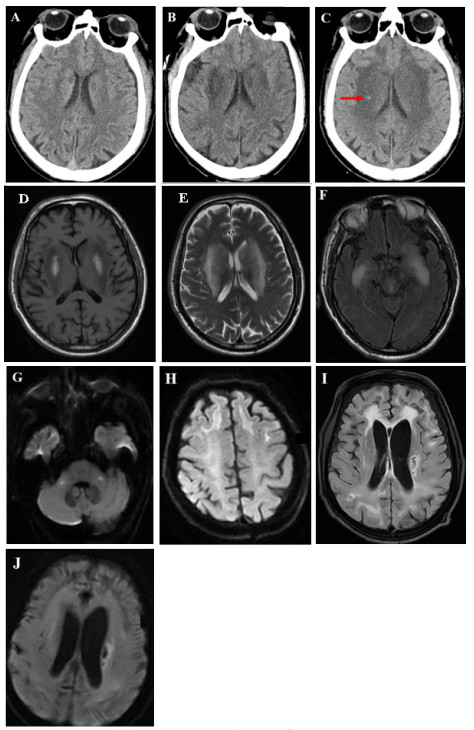
| 注:(A)入院第1天CT示双侧脑室旁见对称性月晕状稍低密度影;(B)入院第5天CT示双侧基底节区对称性低密度灶,较前显著;(C)入院第15天CT示双侧基底节区病灶较前密度减低,新增小片状高密底影,提示小出血灶(箭头所示);(D-H)入院第9天MRI示双侧基底节区呈对称性长T1长T2信号,伴有脑肿胀;FLAIR序列双侧颞叶深部对称性高信号影;DWI序列双侧桥臂、额叶皮层下白质多发斑点片状及条片状高信号影;(I-J)出院第6个月MRI示FLAIR和DWI序列双侧基底节区仍见多发斑点状及条片状异常信号影,较前高信号减低,范围缩小,脑室系统明显扩大,皮层萎缩 图 1 本例患者头颅影像学动态演变 |
|
|
患者入院后即行血液灌流(3次/d,共2 d)清除毒物、连续性肾脏替代治疗纠正内环境紊乱、血管活性药物维持血压、补液促进毒物排泄及对症支持等治疗。中毒后第5天,患者仍深昏迷,GCS评分2T(E1VTM1)。复查头颅CT:双侧基底节区对称性低密度灶,较前片明显,见图 1B。中毒后第9天,意识状况仍无改善,检查头颅MRI:双侧额顶颞枕叶皮层下、基底节区、桥臂多发异常信号,伴脑肿胀,考虑中毒性脑病,见图 1D~图 1H;磁共振动脉自旋标记(arterial spin labeling, ASL):两侧额颞叶皮层下白质区对称性灌注增高,两侧基底节、小脑、枕顶叶对称性灌注减低,符合中毒性脑病改变,见图 2A~图 2C。针对意识障碍治疗予纳洛酮静脉滴注;针对脑水肿予20%甘露醇静脉滴注(每次150ml,第1周每8小时1次,第2周每12小时1次),甲泼尼龙静脉注射(每次40mg,第1周每日2次,第2周每日1次)。中毒后第7天行床旁气管切开,中毒后第15天呼吸循环稳定,停用呼吸机,但仍处于昏迷状态,无气道自洁能力,GCS评分5分(E2V1M2)。中毒后第15天复查头颅CT:双侧基底节区病灶较前密度减低,新增小片状高密度影,提示小出血灶,见图 1C。
|
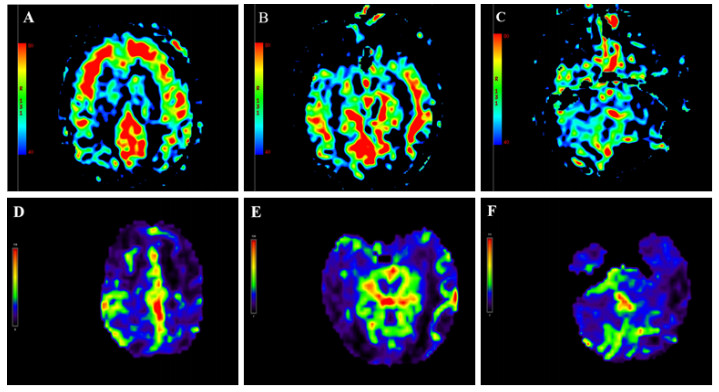
| 注:(A-C)中毒第9天,头颅ASL显示双侧额叶、颞叶皮层下白质区对称性灌注增高,双侧小脑半球灌注减低;(D-F)中毒后第6月头颅ASL显示双侧额叶、枕叶、小脑半球灌注弥漫性减低;图中红色代表高灌注,蓝色代表低灌注,黄色代表两者之间 图 2 本例患者头颅ASL灌注成像动态变化 |
|
|
患者中毒后第20天出院,并转至本地康复医院继续治疗,方案包括高压氧促进脑功能恢复、药物预防癫痫发作,辅以低频电刺激、电动起立床训练、针灸等康复治疗。康复过程中患者持续经鼻饲进食,大小便无法自控,中毒后第3个月GCS评分7分(E2V2M3)。坚持以上康复方案,中毒后第6个月,GCS评分10分(E3V3M4)。复查头颅MRI:双侧额顶枕叶皮层下可见少许斑点片状及条片状DWI稍高信号影,较前高信号减低,范围缩小,脑室系统明显扩大,皮层萎缩,见图 1I ~图 1J。磁共振ASL:双侧额顶枕叶、小脑半球灌注弥漫性减低,损害范围较前扩大,见图 2D~图 2F。动态随访,中毒后第10个月,患者意识状况稍改善,能自主睁眼,简单应答,对刺痛能明确定位,能经口进食,GCS评分12分(E4V3M5)。随访至中毒后第15个月,患者神经功能较前不再有显著变化。
2 讨论哒螨灵是线粒体氧化复合物Ⅰ的抑制剂,影响线粒体电子传递链,经口摄入后可出现胃肠道症状、肝肾功能不全、乳酸酸中毒及心肌损害等[1-2]。同时,因其具有亲脂性,可穿过血脑屏障,导致神经元受损,出现神经系统症状[3]。目前哒螨灵中毒引起中毒性脑病的报道较为少见,其机制亦不明确。研究表明,电子传递链复合物Ⅰ抑制剂与帕金森病的发病相关,作为该抑制剂代表药物之一的哒螨灵可用于帕金森病的动物造模,在动物研究中哒螨灵暴露可导致线粒体产生过量的超氧阴离子,诱导神经元功能障碍和死亡[4-5],以上机制可能与哒螨灵摄入导致的中毒性脑病有关。
中毒性脑病是由药物或毒物引起的中枢神经系统器质性病变,主要累及脑白质,同时也可侵犯灰质结构及部分神经核团,临床表现多样[6]。影像学检查对于中毒性脑病具有重要价值,能够明确病变范围及脑实质受累程度,并为临床诊疗方案提供关键依据。急性期的脑CT扫描常表现为皮层下白质弥漫性对称性低密度信号,脑组织肿胀[7];MRI在评估中毒性脑病方面比CT更为敏感,常表现为T2WI、FLAIR和扩散加权像(DWI)上皮层下白质对称性高信号病变,此外,某些毒物还会引起双侧小脑齿状核、苍白球、内外囊、丘脑出现异常信号强度[7-10]。本例哒螨灵中毒患者急性期主要表现为意识障碍,影像学提示双侧额顶颞枕叶皮层下、基底节区、桥臂多发病变,表明严重哒螨灵中毒所致神经系统损害累及范围较广。随访至半年后,上述神经系统损害在MRI上仍然存在,且伴随严重的皮层萎缩,脑室扩大,提示患者神经影像发生持续性不可逆性的损害。但患者经治疗后意识状况有一定程度好转,其GCS评分在出院后的康复过程中存在缓慢改善的趋势。已有报道在一氧化碳中毒性脑病的患者中,CT或MRI检查结果并不能准确反应病情的轻重和转归[11],这一结论与本案例相似。
目前关于中毒性脑病局部脑血流变化的研究较少,本例患者进行了脑灌注检查,以期为中毒性脑病提供更多具有特征性的诊断依据。有研究[12]对3例甲苯中毒性脑病患者进行了磁共振ASL检测,结果发现中毒组所有感兴趣区平均脑血流量值和正常对照组无差异。然而,川玲等[11]通过核素脑血流灌注显像的方法对46例中毒性脑病患者进行观察,发现大部分患者存在不同程度的局限性或弥漫性脑血流灌注减低。本例哒螨灵中毒患者磁共振ASL检测显示急性期不同部位脑血流变化趋势不一,表现为双侧额颞叶皮层下白质区对称性高灌注,基底节、小脑、枕顶叶对称性低灌注,6个月后复查发现全脑多部位呈弥漫性低灌注。通常,中毒性脑病伴随脑细胞水肿和血管内皮细胞肿胀,影响脑的血液循环,导致低灌注。本例中毒性脑病急性期部分脑白质区呈现高灌注,其原因尚不明确,可能与中毒后这些区域脑实质发生充血肿胀、血流速度增快有关[13]。
目前针对哒螨灵中毒无特效解毒药物。针对口服中毒者,尽早洗胃、导泻、清除毒物可能有助于减少其对神经系统的损伤。哒螨灵具有亲脂性特点,血液灌流可作为首选的血液净化方式,以清除血液循环中的毒物分子。研究表明,中毒性脑病患者急性期和亚急性期可发生脑细胞毒性水肿和血管源性水肿[14],因而此类患者病程中需关注脑水肿变化。除甘露醇等脱水剂外,可使用糖皮质激素减轻细胞的炎症反应及脑水肿程度[15]。高压氧也是治疗中毒性脑病的措施之一,其主要作用机制包括:提高血氧分压,增加脑组织氧贮备量;增加脑组织内有氧
氧化和ATP的产生,促进脑组织修复;改善脑血管壁的营养,促使血管内膜的修复等[16]。本例哒螨灵中毒性脑病患者早期即进行高压氧干预,同时联合了其他康复措施,且维持了较长疗程,在上述治疗基础上患者的意识状况有一定程度改善。
如上所述,虽本例哒螨灵所致中毒性脑病患者GCS评分在出院后有一定程度改善,但影像学仍表现为较为严重的不可逆性的损伤。中毒性脑病的预后并非单一因素决定,它受毒物的毒性程度、服毒量、患者自身状况以及临床干预的时效性与规范性等多种因素影响。针对中毒性脑病,应及时实施毒物清除及系统的神经保护与生命支持,选择适宜疗程的高压氧等康复措施,以最大程度减轻神经功能损害和促进恢复。
利益冲突 所有作者声明无利益冲突
| [1] | Goswami P., Gupta S., Biswas J., et al. Endoplasmic reticulum stress plays a key role in rotenone-induced apoptotic death of neurons[J]. Mol Neurobiol, 2019, 56(9): 6654-6655. DOI:10.1007/s12035-019-01674-x |
| [2] | 杜家年, 孙峰, 张劲松. 哒螨灵中毒致脑出血一例[J]. 中华急诊医学杂志, 2020, 29(11): 1490-1491. DOI:10.3760/cma.j.issn.1671-0282.2020.11.022 |
| [3] | 张辉, 王慧娟, 熊高锋, 等. 血液净化治疗成功救治哒螨灵中毒2例[J]. 中华劳动卫生职业病杂志, 2024, 42(5): 381-383. DOI:10.3760/cma.j.cn121094-20230417-00134 |
| [4] | Morton KS, George AJ, Meyer JN. Complex I superoxide anion production is necessary and sufficient for complex I inhibitor-induced dopaminergic neurodegeneration in Caenorhabditis elegans[J]. Redox Biol, 2025, 81: 103538. DOI:10.1016/j.redox.2025.103538 |
| [5] | Charli A, Jinjun H, Anantharam V, et al. Alterations in mitochondrial dynamics induced by tebufenpyrad and pyridaben in a dopaminergic neuronal cell culture model[J]. Neurotoxicology, 2016, 53: 302-313. DOI:10.1016/j.neuro.2015.06.007 |
| [6] | Cai D, Kuang L, Hu F, Shen Y. Abnormalities along the cortico-medullary junction on brain MRI caused by 1, 2-dichloroethane-induced toxic encephalopathy[J]. BMC Neurol, 2024, 24(1): 447. DOI:10.1186/s12883-024-03952-1 |
| [7] | Chen S, Zhang Z, Lin H, et al. 1, 2-Dichloroethane-induced toxic encephalopathy: a case series with morphological investigations[J]. J Neurol Sci, 2015, 351(1/2): 36-40. DOI:10.1016/j.jns.2015.02.020 |
| [8] | 方红丽, 叶小军, 王小川, 等. 中毒性脑病35例临床特征和预后分析[J]. 中华危重症医学杂志(电子版), 2020, 13(3): 207-210. DOI:10.3877/cma.j.issn.1674-6880.2020.03.009 |
| [9] | 程留慧, 王道清, 张保朋, 等. 中毒性脑病的影像学表现[J]. 中国中西医结合影像学杂志, 2017, 15(4): 465-467. DOI:10.3969/j.issn.1672-0512.2017.04.026 |
| [10] | Wang J, Jian T, Yu G, et al. Case Report: Evaluating toxic encephalopathy from occupational 1, 2-dichloroethane exposure: magnetic resonance imaging contributions[J]. Front Toxicol, 2025, 7: 1557995. DOI:10.3389/ftox.2025.1557995 |
| [11] | 川玲, 赵文锐, 朱家瑞, 等. 评价99Tcm-ECD脑血流灌注显像检测中毒性脑病局部脑血流变化的价值[J]. 海军总医院学报, 2003, 16(4) 219-221, 256. DOI:10.3969/j.issn.1009-3427.2003.04.009 |
| [12] | 廖海波, 肖新兰, 戴中强, 等. 甲苯中毒性脑病磁共振及功能性成像特征分析[J]. 临床放射学杂志, 2014, 33(7): 1096-1100. DOI:10.13437/j.cnki.jcr.2014.07.033 |
| [13] | Lipkin WI, Hornig M. Diagnostics and discovery in viral central nervous system infections[J]. Brain Pathol, 2015, 25(5): 600-604. DOI:10.1111/bpa.12277 |
| [14] | Zhan F, Zheng W, Liu L, et al. Diagnosis and prognosis evaluation of 1, 2-dichloroethane encephalopathy-magnetic resonance imaging combined with diffusion tensor imaging and magnetic resonance spectroscopy study[J]. Neurol India, 2011, 59(1): 108-110. DOI:10.4103/0028-3886.76884 |
| [15] | 范川, 陈先文. 有机溶剂中毒性脑病研究进展[J]. 中华神经科杂志, 2014, 47(1): 55-58. DOI:10.3760/cma.j.issn.1006-7876.2014.01.016 |
| [16] | 穆杭. 早期高压氧冶疗对CO中毒性脑病防治的临床观察[J]. 实用临床医学, 2005, 6(2): 32-33. DOI:10.3969/j.issn.1009-8194.2005.02.015 |
 2026, Vol. 35
2026, Vol. 35